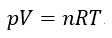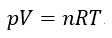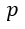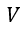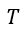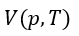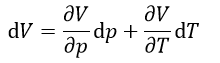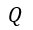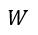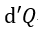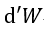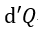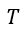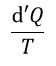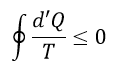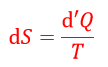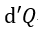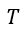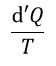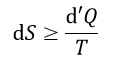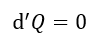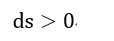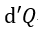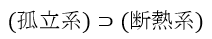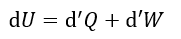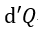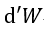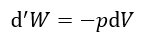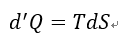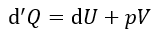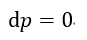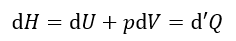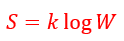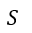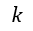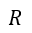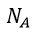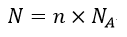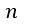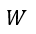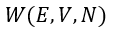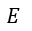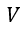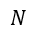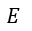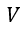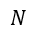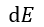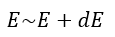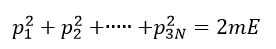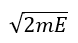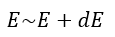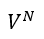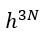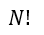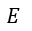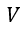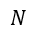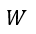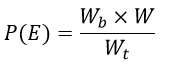以下、共通して温度一定で、エネルギーは両容器で交換する(容器系のエネルギーは一定では
ない)4つのケースを簡単に示します。
|
(1) | 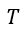 | , | 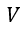 | , | 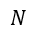 | 一定で | 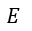 | のみ熱浴系との間で出入りして変化する場合
|
正準集団の手法を用います。結果のみ示します。
規定化関数を
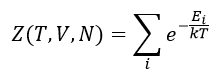 | (16)
|
とおくと、出現確率は
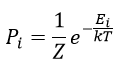 | (17)
|
そして熱力学の内部エネルギーはこのエネルギーの平均値となり、
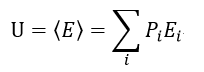 | (18)
|
となります。エントロピーは
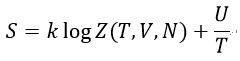 | (19)
|
となります。
|
パラメータが | 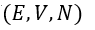 | ⇒ | 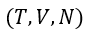 | となっています。
|
|
(2) | 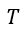 | , | 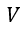 | 一定で | 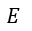 | のみならず | 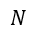 | も熱浴系との間で出入りして変化する場合
|
正準集団の手法を用います。結果のみ示します。
規定化関数を
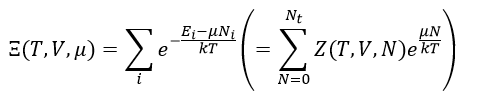 | (20)
|
とおくと、出現確率は
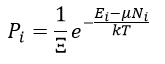 | (21)
|
また、
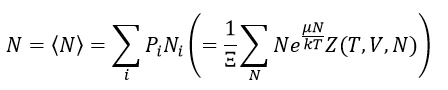 | (22)
|
となるので、エントロピーは
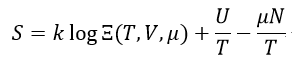 | (23)
|
となります。ここで、μは化学ポテンシャルです。
|
パラメータが | 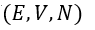 | ⇒ | 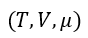 | となっています。
|
規定化関数を
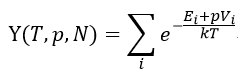 | (24)
|
としますと、出現確率は
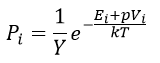 | (25)
|
また、
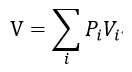 | (26)
|
となるので、エントロピーは
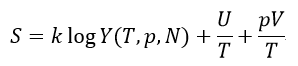 | (27)
|
となります。
|
パラメータが | 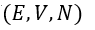 | ⇒ | 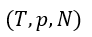 | となっています。
|
規定化関数を
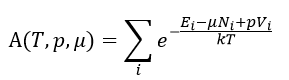 | (28)
|
としますと、出現確率は
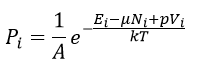 | (29)
|
となるので、エントロピーは
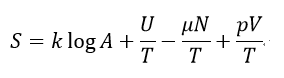 | (30)
|
となる。
|
パラメータが | 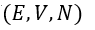 | ⇒ | 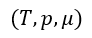 | となっています。
|
以上の式を見ると、次の形になっています。
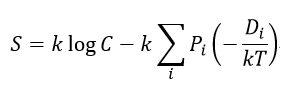 | (31) |
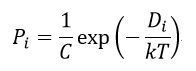 | (32)
|
(32)より、
となるので、(31)に代入すると
となります。もう一度書きますと
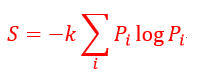 | (33)
|
というよく見る式が導出されたわけです。
ちょっと誤解していましたが、エネルギーも一定として論じた小正準集団はどうなの?と思ったの
ですが、この(33)式はそれも含むことがわかりました(説明は省略)。
EMANさんによれば、教科書によっては最初からこの(33)式を出しているものもあるそうです。
それで、わかりました。巷で言われている話は、「エントロピー増大則」とこの式から敷衍したも
のだと。
しかしながら、この式は、あくまで、前述のような考察から、数学的に導かれたものでしかありま
せん。何もないところから突然ぽっと出てきたものでも何でもないわけです。
この式に至るまでの理論過程においては、かなり近似的考察を重ねています。邪魔な部分を値
が小さいとからとしてneglectもしています。証明できないからと「原理」と言う名称を使う「等重率
の原理」という概念も入っています。そして、私が気になっているのは「孤立系」という仮定の元に
論じられていることです。
したがって、いくら「美しい式」が導出されようと、「美しいから」といって、「自然の要請」というのは
単なる思い込みではないかと思うのです。「自然」がそれらのいわば人間がなした「仮定」通りか
どうかなど証明されていないからです。
繰り返しますが、そもそも、エントロピーというのは熱力学で定義されたものですが、あくまで、人
為的に定義された概念です。全ての人が自然に思念できるようなものではありません。
しかも前述のように、「エントロピー増大」は熱力学の理論的な結論ですが、そこでは「断熱系」と
いう条件が厳然と入っているのです。全ての場合に成り立つものではないのです。
(33)式は断熱系より厳しく断熱系を包含する「孤立系」という場合で理論展開した結果です。そし
てその式の元になった(16)式は前述のように熱力学から論理的に導出されたものではないという
ことです。その意味で、区別して「統計力学的エントロピー」と称しているということは前述しました。
近年、情報理論の方面で、1と0というビット単位関連が丁度、ボルツマンの(16)式と類似している
ということから、「情報エントロピー」という概念が生まれています。kの値は異なりますが。
結局のところ、「エントロピー増大」というのは、元々の定義である熱力学については、「熱力学
の第二法則」という「言葉」だけが使われ、後は、(33)式、そして、補填的に情報エントロピーか
ら「思いついた」ものを、いかにも「自然の法則」であるかのように論じているというのが事実で
はないでしょうか?
以上より、例えば「時間の矢は熱力学の第二法則より説明できる」というのは、論理的でない思
い込みから来るフレーズであると考えます。
また、ごみが散らかることをもって、エントロピー増大を説明するのは、本末転倒かつ真の証明
にもなっていない議論だと思います。
要するに「エントロピー増大」というのは、摩訶不思議な自然の法則でもなんでもなく、単なる一
つの科学理論以上のなにものではないと私は思うのです。
元々は、熱力学第二法則に関するある議論対立を目にして真相を知りたいと思って調べたので
すが、私自身浅学菲才の身、付け刃的な今回調べた知識の中ではその答えは見つかりません
でした。もっとも、私は上記の自分自身の結論からその議論自体おかしな話だと思っていますか
らどちらがどうのというのではなく、そこに持ち出されていた「科学的」な部分への興味です。
もう少し調べて見る必要があります。
('16/7)
目次に戻る
|